|
İÇ HASTALIKLARI Dergisi 2013; 20: 1-11
DERLEME
|
İnfeksiyon Hastalıklarında Antipiretik Kullanımı
Uzm. Öznur AK, Doç. Dr. Serap GENÇER
Dr. Lütfi Kırdar Kartal Eğitim ve Araştırma Hastanesi, İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Kliniği, İstanbul
Antipiretik tedavi vücut ısısını normal sınırlara düşürmek amacıyla yapılan tedavidir. Çok yüksek vücut ısısının zararlarına rağmen infeksiyon hastalıklarında ortaya çıkan ve asla insanlarda 41°C'yi aşmayan yüksek vücut ısısını düşürmenin yararı bugün hala tartışılmaktadır. Güneş çarpması veya yüksek ısıya maruz kalma gibi sebeplerle ortaya çıkan hipertermi durumunda vücut ısısı sıklıkla zararlı seviyelere yükselebilir (1). Sağlıklı gönüllülerin dört saate kadar uzun bir zaman periyodunda 42°C'lik vücut ısısına karşı koyabildikleri bildirilmiş olmasına rağmen bir kısım hastada vücut ısısında az miktarda artış bile zararlı olabilmekte ve bu yüzden ateşin baskılanması gerekebilmektedir (2).
Antipiretik tedavi uygulamasının orijini tam bilinmemekle beraber günümüzde de kullanılan soğuk uygulama veya banyoların MÖ 323 yılında uygulandığı, ilaç tedavisi olarak bitkisel tedavilerin yaklaşık 2000 yıldan daha uzun zamandır kullanıldığı bilinmektedir (3,4,5). Sümerler, Asurlular ve eski Mısırlılar özellikle söğüt ağacı (willow bark) kabuğu başta olmak üzere çeşitli bitkileri ateş düşürücü ve romatizmal hastalıklarda ağrı kesici olarak kullanmışlardır. İlk bilimsel olarak salisilattan zengin söğüt kabuğunun antipiretik olarak yararını Reverend Edward Stone 1763 yılında Londra'da açıklamıştır. 1829 yılında Henry Leroux salisini hidrolize ederek antipiretik özelliğini göstermiş, 1838 yılında Raffaela Piria salisilik asidi oluşturmuş, 1852 yılında Gerland ilk olarak salisilik asidi sentezlemiştir. 1899 yılında Felix Hoffman tarafından üretilen asetilsalisilik asit sentezlenmiş ve antipiretik ilaç olarak Aspirin piyasalara sunulmuştur (3,4,5,6,7).
Bu dönemde paraaminofenol derivesi olan asetenilid, fenasetin ve pirazolon bileşikleri de geliştirilmiş, ancak asetanilid ve fenasetin kısa sürede hepatotoksisite nedeniyle piyasadan çekilmiştir (3,8). 1948 ve 1949 yıllarında Brodie ve Axelrod majör metaboliti fenasetin olan parasetamolün 1893 yılında antipiretik olarak kullanıldığını ve fenasetine göre toksik etkisinin daha az olduğunu, antipiretik ve analjezik olarak fenasetinin yerini alabileceğini bildirmişlerdir. Asetilsalisilik asitten farkı ise antiinflamatuvar etkinliğinin olmamasıdır (8). On dokuzuncu ve yirminci yüzyılda nonsteroid antiinflamatuvar ilaçlar (NSAİİ)'daki gelişmeler devam etmiştir. Bu ilaçların etki mekanizması tam olarak bilinmemekte iken, 1971 yılında John Vane siklooksijenaz (COX) enzimi aracılığıyla prostaglandin (PG) sentezini inhibe ederek etki ettiklerini bildirmiş ve 1970 dönemi prostaglandin öncesi dönem iken, daha sonrası prostaglandin dönemi olarak tanımlanmıştır. 1990'lı yıllarda yapılan moleküler çalışmalarla siklooksijenaz enziminin iki farklı alt grubunun olduğu gösterilmiş ve bu enzimlere selektif nonsteroid antiinflamatuvar inhibitörler geliştirilmiştir (9).
ANTİPİRETİK TEDAVİDE YARAR-ZARAR İKİLEMİ
Ateşi düşürmenin gerçek yararı bilinmemekle birlikte bazı hasta gruplarında çeşitli gerekçelerle ateşin zararlı etkileri önlenmeye çalışılmaktadır. Bu gerekçelerden biri çocuklarda febril konvülziyonları önlemektir. Özellikle 3 ay-5 yaş arasındaki çocuklarda ateş atakları sırasında %14 kadar yüksek bir oranda konvülziyon rapor edilmiştir (10). Birçok çocuk konvülziyon sırasında 39°C ve üzeri vücut ısısına sahip olmasına rağmen birçoğu daha sonraki zamanlarda daha yüksek ateşi konvülziyonsuz olarak tolere eder (11,12). Ne yazık ki, antipiretik tedavinin febril konvülziyonların rekürrensine karşı koruyucu olduğu bugüne kadar gösterilmemiştir (13). Camfield ve arkadaşlarının yürüttüğü randomize çift-kör çalışmada ilk febril konvülziyondan sonra rekürren konvülziyonu engellemek için tek doz fenobarbital ve antipiretikle plasebo ve antipiretik karşılaştırılmıştır (14). Fenobarbital ve antipiretikle tedavi edilen çocuklarda febril konvülziyon rekürrens oranı %5 iken, plasebo ve antipiretik verilenlerde %25 olmuş, böylece tek doz fenobarbitalin antipiretik tedaviden daha etkili olduğu gösterilmiştir. Daha yakın zamanda yapılan çalışmalarda ateşli çocuklara febril konvülziyon rekürrenslerine karşı profilaktik olarak parasetamol verilmiş ve yüksek dozlarda (15-20 mg/kg her 4 saatte bir) bile febril konvülziyon rekürrens oranlarını azaltmada başarısız olduğu gösterilmiştir (15,16).
Antipiretik tedavi vermenin bir diğer gerekçesi ateşin metabolik maliyetini azaltmak olabilir. Altta yatan kardiyovasküler veya pulmoner hastalıkları olan hastaların ateşin istenmeyen etkilerine karşı özellikle duyarlı olabildikleri gösterilmiştir (17). Vücut ısısının artmasıyla birlikte artan metabolik talep sonucunda oksijen tüketimi, solunum dakika hacmi ve solunum sayısı artmaktadır. Vücut ısısının 37°C'nin üzerinde her 1°C'lik artışı oksijen tüketimini %13 artırır. Özellikle titreme fazı sırasında metabolik hızın artmasıyla, norepinefrin aracılı periferal vazokonstrüksiyon ve artmış arteryel kan basıncıyla ateşin metabolik maliyeti azımsanamaz (18). Bu metabolik etkilerin kardiyovasküler ve pulmoner fonksiyon üzerinde potansiyel istenmeyen sonuçlarından dolayı bu hastalarda antipiretik kullanımından yarar beklenmesine rağmen böyle bir tedavinin risk-yarar oranı henüz belirlenmemiştir (19). Ateşin metabolik maliyeti fizyolojik yararından fazlaysa antipiretik tedavi uygulanabilir.
Antipiretik tedavi vermenin bir başka gerekçesi, belki de esas hedefi, hasta konforunu artırmaktır. Ancak, kontrollü etkinlik çalışmaları bu iddianın doğruluğunu ve ilaç toksisitesi veya hastalık seyri üzerindeki yan etkiler anlamında maliyetini henüz saptamamıştır. Parasetamolün suçiçeği geçirmekte olan çocuklarda lezyonların kabuklanma süresini uzattığı, hem parasetamolün hem de asetilsalisilik asidin rinovirüs infeksiyonlu yetişkinlerde serum nötralizan antikor yanıtını süprese ederken viral atılım ve nazal semptom ve bulguları artırdığı ve antipiretik ilaçların influenza A infeksiyon seyrini uzattığı çeşitli çalışmalarla gösterilmiştir (20,21,22,23). Antipiretik ilaçların toksisite ve yan etkileri olduğu kadar semptomatik rahatlama sağlarken ateşten sorumlu hastalığın seyrini olumsuz etkileyebileceği de bilinmelidir (19).
Ne yazık ki, belli antipiretik ilaçlar koroner arter hastalarında koroner vazokonstrüksiyona da yol açar. Friedman ve arkadaşları böyle hastalarda intravenöz indometazin (0.5 mg/kg) verilmesinden sonra ortalama arteryel basınçta, koroner vasküler direncinde ve miyokardiyal arteriyovenöz oksijen farkında ciddi artışlar olduğunu, koroner kan akımının eş zamanlı olarak azaldığını ve böylece miyokardiyal oksijen talebinin arttığını göstermişlerdir (24). İndometazinin vazokonstrüktör etkisi muhtemelen vazodilatör prostaglandinlerin sentezini bloke etme yeteneğine bağlıdır. Diğer NSAİİ'lerle karşılaştırıldığında COX-2 selektif NSAİİ'lerin asetilsalisilik asit almayan hastalarda kardiyovasküler trombotik olay riskini artırdığı görülmektedir (25).
Sepsisin bazı hayvan modellerinde siklooksijenaz inhibe eden antipiretik ilaçlar en kısa sürede verildiğinde korunma sağlar. Geniş bir klinik çalışmada Bernard ve arkadaşları siklooksijenaz inhibitörü ibuprofen ile 48 saat intravenöz tedavinin vücut ısısını, kalp hızını, oksijen tüketimini ve laktik asit kan seviyelerini azalttığını fakat organ yetmezliği veya 30 günlük mortalite insidansını azaltmadığını rapor etmişlerdir (26). Daha yakın zamanlı bir retrospektif sepsis çalışmasında Eichacker ve arkadaşları sadece yüksek ölüm riski olan septik hastalarda antipiretik ajanların yararlı etkisi olduğunu göstermişlerdir (27). Böylece, bazı deneysel modellerde elde edilen umut verici sonuçlara rağmen antipiretik ajanların bakteriyel sepsis tedavisinde klinik olarak ancak sınırlı etkisi olduğu gösterilmiştir (19).
Antipiretik ilaçlara yanıt vermeyen ateşi düşürmek için ciddi derecede hasta olanlarda yaygın olarak kullanılan dışarıdan soğutmanın, eğer titreme engellenebilirse oksijen tüketimini %20 oranında azalttığı gösterilmiştir. Eğer titreme engellenmezse dışarıdan soğutma oksijen tüketimini azaltmaktan ziyade artışına yol açar (28). Hatta kardiyovasküler hastalığı olan ateşli hastalarda soğuk presör yanıtı indükleyerek hasta koroner arterlerin vazospazmına yol açma riski vardır (29,30). Tüm bu sebeplerle, antipiretiklere yanıtsız ateşi kontrol etmede daha gerçekçi yaklaşımın seçilmiş cilt yüzeylerini (örn. alın bölgesi) soğutmak yerine, vazokonstrüksiyonu ve titreme eşiğini azaltmak için ısıtmak olduğu önerilmektedir (31).
Ateşin metabolik yükünün fizyolojik yararını aşabileceği, antipiretik tedavinin ateşli hastalığın seyrini olumsuz etkilemeden semptomatik yarar sağlayabileceği veya antipiretik rejimin toksisitesinin yararlı etkilerinden daha az olması klinisyenler tarafından uzun zamandır tartışılmaktadır. Ancak, tüm bu bakış açılarının doğruluğunu destekleyen çok sınırlı bilimsel veri bulunmaktadır (19). Eğer bu birikim mevcut olsaydı, bugün antipiretik tedaviyi savunmak daha kolay olacaktı. Öte yandan, ateşin konağın infeksiyona karşı direnme yeteneğine katkı sağlayan önemli bir savunma mekanizması olduğunun ise kanıtı bulunmaktadır (32).
ANTİPİRETİK TEDAVİ ENDİKASYONLARI ve UYGULANMASI
Uzun yıllardır tıp pratiğinde ateşi düşürmenin yollarını arama konusunda yoğun çaba gösterilmesine rağmen, antipiretik tedavilerin esas yararları ve göreceli riskleriyle ilgili bilimsel veriler ne yazık ki sınırlıdır (33). Dolayısıyla antipiretiklerin endikasyonlarını belirlerken ateşin yararına karşı metabolik maliyeti, antipiretiklerin yararına karşı zararları dikkate alınarak her hasta ve duruma göre ayrı karar verilmelidir. Örneğin; kritik hastalarda veya metabolik rezervleri sınırlı kronik hastalıklı çocuklarda, ateşin artmış metabolik baskısını tolere edemeyecekleri için ateşi düşürmek uygun bir yaklaşım olabilir (34,35). Yeterli kanıt olmamasına rağmen birçok pediatrist aşılama öncesinde parasetamol veya ibuprofen önermektedir. Ancak, yakın zamanda yapılmış bir çalışma; öncesinde antipiretik verilen hastalarda aşılara karşı immün yanıtın azalma olasılığını göstermektedir (36).
Standart antipiretik ilaç dozlarının kısa süreli kullanımı düşük toksisite riski taşımaktadır. Eğer kontrendikasyon yoksa bu tür ilaçlar ateşli hastalarda semptomatik rahatlama sağlamak, kardiyovasküler hastalık veya pulmoner hastalığı olanlarda ateşin metabolik taleplerini azaltmak ve yaşlı hastalarda ateşin indüklediği mental disfonksiyonu önlemek veya hafifletmek için kullanılabilir. Ancak, tekrarlayan titreme riskini ve antipiretiklerin indüklediği ısı dalgalanmalarını en aza indirmek için belli bir seviyenin üzerindeki ateşi düşürmeye yönelik keyfikeder uygulama yerine, ani ateş ataklarını önlemek için antipiretikler düzenli aralıklarla verilmelidir (19).
En yaygın ve sıklıkla etkili biçimde kullanılan antipiretik ajanlardan biri parasetamoldür. Antipiretik dozu yetişkinlerde günlük 325-1000 mg oral, çocuklarda 4-6 saatte bir 10-15 mg/kg oraldir. Parasetamolün intravenöz formu birçok ülkede kullanılmaktadır. Avrupa'da 2002 yılından beri kullanılmakta olan intravenöz parasetamol Amerika Birleşik Devletleri (ABD)'nde çok kısa bir süre önce "Food and Drug Administration (FDA)" onayı almıştır. İntravenöz parasetamolün (1000 mg) antipiretik etkisi 30 dakikada ortaya çıkmakta ve en az altı saat sürmektedir. Özellikle postoperatif dönemde ağrıyı azaltmak ve aynı zamanda postoperatif ateşi düşürmek için kullanılmaktadır (37).
Yapılan çalışmalarda daha uzun klinik etkisi olduğu görülen bir diğer antipiretik ajan ibuprofendir. Karşılaştırmalı çalışmalarda ibuprofenin (10 mg/kg) en az parasetamol (15 mg/kg) kadar, hatta belki de daha etkili olduğu gösterilmiştir (34). Çocuklarda en sık kullanılan tedavi parasetamol ve ibuprofen kombinasyonudur. Sarrell ve arkadaşlarının yürüttüğü randomize, çift-kör çalışmada 6-36 ay arası 464 çocukta parasetamol (her 6 saatte bir 12.5 mg/kg) veya ibuprofen (her 8 saatte bir 5 mg/kg) monoterapisi ile her ikisinin değişimli kullanımının antipiretik etkinliği karşılaştırılmış, üç günlük dört saatte bir olmak üzere değişimli kullanımının ateşi düşürmede her iki monoterapiden daha etkili olduğu gösterilmiştir (38).
Ateşi düşürmede sıklıkla kullanılan bir diğer ajan asetilsalisilik asittir. Bu ilaç 4-6 saatlik aralarla sürekli uygulama şeklinde verilmektedir. Antipiretik doz yetişkinlerde 4-6 saatte bir 350-650 mg oral, çocuklarda 4 veya 6'ya bölünecek şekilde 50-75 mg/kg/gün dozunda verilmelidir. Total doz 3600 mg'ı aşmamalıdır. Antiplatelet etkisinden dolayı infektif endokarditlerde vejetasyon oluşumu ve emboli riskini azaltmak için tercih edilmektedir. Çocuklardaki viral infeksiyonlarda Reye sendromuna yol açabileceğinden kaçınılması önerilmektedir.
Bilinen istenmeyen etkilerinin yanında antipiretiklerin dikkatli kullanılması gerekmektedir. Parasetamolün metaboliti, N-asetilimidokinon, intrensek hepatotoksik etkileri olduğu için etanol gibi hepatotoksinlerle birlikte alınmamalıdır. Rifampin, fenitoin gibi sitokrom P-450 enzim sistemini indükleyen ilaçlarla birlikte kullanımı toksisite riskini artırabilmektedir. Antipiretik ilaçların her birinin kendi toksisite riskini taşıdığı ve yakınmaların şiddetini azaltırken ateşten sorumlu hastalığın seyrini uzatabileceği bilinmelidir. Dışarıdan soğutmanın soğuk presör yanıtı indükleme riskinden dolayı febril hastalara uygulanmasına şüpheyle yaklaşılmalı ve uygulanacağı zaman titremenin engellenmesine dikkat edilmelidir. Ancak, titreme engellense bile soğuk presör yanıtının engellenmesinin garantisi yoktur. İndometazinin koroner arter hastalığında koroner vazokonstrüksiyona yol açma kapasitesinden ve kardiyovasküler trombotik olayların artmış riskinden dolayı koroner arter hastalarında dikkatlice kullanılmalıdır (19).
ANTİPİRETİK İLAÇLARIN SINIFLAMASI
Günümüzde antipiretik olarak kullanılan ilaçları iki ana grupta toplamak mümkündür (19):
1. Kortikosteroidler,
2. NSAİİ'ler.
Kortikosteroidler
Genelde antipiresis için kullanılmamasına rağmen, direkt ve indirekt mekanizmalarla ateşi baskılar. Glukokortikoid reseptörü kapsayan etkileşimler vasıtasıyla pirojenik sitokinler ve indüklenebilir siklooksijenaz transkripsiyonunu bloke eder (39,40). Sitokin reseptörlerinin sentezini azaltır ve lipokortin-1'i indükleyerek prostaglandin sentez yolundaki kritik enzim olan fosfolipaz A2'nin aktivitesini inhibe eder (40).
NSAİİ'ler
Tüm dünyada yaygın olarak kullanılan ilaçlar arasındadır. Bu grup ilaçların analjezik, antiinflamatuvar ve antipiretik etkinlikleri vardır.
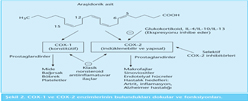
Etki mekanizmaları: NSAİİ'lerin etki mekanizmasıyla ilgili olarak 1971 yılı öncesi çok az bilgi varken 1971 yılında Vane, siklooksijenaz veya prostaglandin endoperoksidaz (PGHS) enzimi aracılığıyla prostaglandin sentezini inhibe ederek etki ettiklerini göstermiştir. Siklooksijenaz enzimi araşidonik asitten orijinini alan prostaglandin, tromboksan ve prostasiklin gibi biyoaktif bileşiklerin sentezindeki kritik enzimdir. Lipooksijenazla birlikte inflamasyon, ağrı ve diğer biyolojik süreçlerde rol alır (8,41,42,43,44). Prostaglandin sentezinin ilk basamağı hücre membranındaki fosfolipidlerden fosfolipaz A2 aracılığıyla araşidonik asidin sentezlenmesidir (Şekil 1). Araşidonik asit siklooksijenaz enzimi aracılığıyla prostaglandinlere, lipooksijenaz enzimi aracılığıyla lökotrienlere dönüşür. NSAİİ'ler siklooksijenaz enzimini inhibe eder, lipooksijenaz enzimi üzerine etkileri yoktur.
Siklooksijenaz enziminin siklooksijenaz ve peroksidaz aktif bölgeleri olmak üzere iki katalitik bölgesi vardır. Siklooksijenaz aktif bölge ile önce araşidonik asitten PGG2, peroksidaz aktif bölge ile PGG2'den PGH2 oluşur. PGH2'den de tromboksan sentetaz ile tromboksan A2 ve prostasiklin sentetaz ile prostasiklin (PGI2) oluşmaktadır (Şekil 1).
Prostaglandinler vücutta birçok dokuda çoğu hücre tarafından sentezlenmektedir. PGE2 ve prostasiklin inflamasyonun esas mediyatörleridir. Prostaglandinlerin inflamasyon dışında sindirim sistemi üzerinde sitoprotektif etkileri ve böbrek fonksiyonlarını düzenleme görevleri de vardır (43,44).
Siklooksijenaz enzimi ilk olarak 1976 yılında izole edilmiştir (42,45). 1990'lı yıllara kadar yalnızca bir siklooksijenaz enzimi olduğu düşünülürken 1990 yılında yapılan moleküler çalışmalarla iki farklı siklooksijenaz enzimi olduğu gösterilmiştir. Bu enzimler; COX-1 konstitütif enzim ve COX-2 indüklenebilir enzim olarak tanımlanır (41,43,44).
COX-1: Sitoprotektif özellikli prostaglandinleri katalize eder. Kolon, böbrek, dalak, mide, karaciğer, akciğer, kalp, beyin, fibroblastlar, makrofaj, vasküler endotel hücreleri, mide mukozası, böbrekler, pankreas, seminal veziküller ve beyin başta olmak üzere birçok dokuda bulunur. Sitokinler, onkojenik uyarılar ve hücresel değişikliklerden etkilenerek sentezlenir. Böbrek ve midede vazodilatör etkili prostanoidleri sentezletir, sistemik vazokonstrüksiyon periyodunda glomerüler filtrasyon ve renal plazma kan akımının sürdürülmesini sağlar. Trombositler üzerinde antitrombotik etkilidir. NSAİİ'lerin gastrik irritasyon gibi istenmeyen etkilerinden daha çok COX-1 sorumludur (41,43,46,47).
COX-2: Normalde inflamatuvar bir uyarı olmadığında saptanamayacak düzeydedir. Proinflamatuvar sitokinler (interlökin (IL)-1β, tümör nekroz faktörü (TNF)-α), lipopolisakkaridler, büyüme faktörleri (fibroblast, epidermal ve trombosit), hormonlar (LH) ve su-elektrolit dengesizlikleri gibi uyaranlarla salınır. COX-1'e göre vücutta daha az dokuda bulunur ve inflamatuvar yanıtın esas mediyatörüdür. Bu indüklenebilir enzim hipotalamus aracılı ateşten sorumludur. NSAİİ'lerin antiinflamatuvar etkisinden esas sorumlu olan da COX-2 inhibisyonudur (41,43).
Şekil 2'de COX-1 ve COX-2'nin fonksiyonları ve bulundukları dokular görülmektedir (43).
COX-1 kromozom 9, COX-2 ise kromozom 1 üzerindeki genlerle kodlanır (43). Garavito ve arkadaşları COX-1'in üç boyutlu yapısını tanımlayarak üç bölge içerdiğini göstermişlerdir. Bu bölgeler epidermal büyüme faktörüne benzer bölüm, membrana bağlanma kısmı ve enzimatik bölümdür (42). Kristalografik çalışmalarda COX-2'nin de benzer olduğu gösterilmiştir. Her iki siklooksijenaz izoformunun yapısı ve katalitik aktiviteleri benzerdir. İkisi de yaklaşık 600 aminoasit içerir ve bu aminoasitler %63 oranında identiktir (8,41,43,45,48). Siklooksijenaz izoenzimleri endoplazmik retikulumda membrana bağlı enzimlerdir. Aktif bölgeleri hidrofobik kanalda lokalizedir. Her ikisinde tirozin 385 ve arjinin 120 önemli bağlanma noktalarıdır. Arjinin 120'nin COX-1 ve COX-2'nin asetilsalisilik asit tarafından inhibisyonunda önemli rolü vardır. COX-1'in arjinin 120 bölgesi karboksilik asit içeren bileşiklerle iyonik bağlanırken, COX-2'nin arjinin 120 bölgesi araşidonik aside hidrojenle bağlanır (5,8,46).
COX-2'nin aktif bölge içeren hidrofobik kanalı COX-1'e göre biraz daha büyük olup, her iki siklooksijenaz enziminin aktif bölgeleri iki aminoasit farklılığı dışında benzerdir. Bu farklılıklar 434 ve 523. pozisyonunda COX-1'de izolösin varken, COX-2'de valinle değişmiştir (3,42,44).
COX-1 enzimi konstitütif enzim olup, fizyolojik homeostazın devamını sağladığı için hormonal stimuluslarla düzenlenir. COX-1 trombosit agregasyonu ve doğum gibi fizyolojik fonksiyonlarda, COX-2 ovülasyon ve implantasyonda rol alır. İnflamasyon ve karsinogenez gibi olaylarda ise her iki enzimin rolü vardır (47). COX-2 hem inflamasyonun başlamasında hem de düzelmesinde etkilidir (44).
Parasetamol COX-1'e yakın olan, aynı genden köken alan ve COX-3 olarak adlandırılan bir üçüncü siklooksijenaz varyantını selektif olarak inhibe eder (49). COX-3'ün keşfinin önemi COX-1 ve COX-2'nin zayıf inhibitörleri olan fakat kolaylıkla santral sinir sistemine penetre olan parasetamol ve diğer NSAİİ'lerin farmakolojik etkilerini açıklamasıdır. Diklofenak veya ibuprofen gibi NSAİİ'ler COX-3'ün güçlü inhibitörleridir fakat etkili konsantrasyonlarda beyindeki COX-3'e ulaşması mümkün değildir (3).
Antipiretiklerin siklooksijenaz enzim inhibisyonu dışındaki etkileri: Asetilsalisilik asit ve NSAİİ'lerin siklooksijenazdan bağımsız antipiretik etkinlikleri de vardır. Asetilsalisilik asit sitokrom P-450'yi indükleyerek araşidonik asit metabolizmasını antipiretik epoksieikosanoidlerin üretimine kaydırarak antipiretik etkisini artırır. Ayrıca, asetilsalisilik asit tarafından COX-2'nin asetilasyonu 15R-hidroksieikosatetraenoik asit üretimini artırır, nötrofiller bunu kullanarak lipoksinleri oluşturur. Bu lipoksinler asetilsalisilik asitten bağımsız olarak güçlü antiinflamatuvar etkinliğe sahiptir (50). Asetilsalisilik asit, sodyum salisilat ve diğer NSAİİ'lerin antiinflamatuvar etkileri siklooksijenaz aktivitesini süprese etmek için gerekli olan dozlardan daha yüksek dozlarda görülür. Bu yüzden pirojenik kaskadda salisilatların tüm etkilerinin açıklanmasında siklooksijenaz bağımlı olmayan fonksiyonlar da öne sürülmüştür: Antiinflamatuvar mediyatörleri stimüle ederler ve inflamasyon bölgesine lökosit geçişini, adezyon moleküllerinin salınımını ve sitokin yapımını azaltırlar (50).
Antipiretik ilaçların etki süresi etki bölgesindeki konsantrasyonlarına ve siklooksijenaz inhibisyonunun reversibl ya da irreversibl olmasına, santral ya da periferik siklooksijenaz inhibisyonuna göre değişir. Asetilsalisilik asit siklooksijenaz enzimi üzerinde irreversibl inhibisyon yapar ve antipiretik etkisi o bölgede yeni enzim sentezlenene kadar devam eder. Diğer NSAİİ'ler ise reversibl siklooksijenaz inhibisyonu yapar ve aktiviteleri etki bölgelerindeki konsantrasyonlarına bağlıdır (50). Parasetamolün santral siklooksijenaz enzim inhibisyonu daha fazla olup, periferik siklooksijenaz inhibitörlerine etkisi zayıftır ve antiinflamatuvar etkinliğinin olmaması da bununla ilgilidir (3).
İki arilpropionik asit deriveleri gibi birçok NSAİİ'nin S- ve R-enantiomeri vardır. R-enantiomeri S-enantiomere göre COX-2'ye 100-500 kat daha az etkilidir ve fonksiyonları in vivo S-enantiomere dönüşümüne bağlıdır. NSAİİ'lerin çoğu bu iki enantiomerin karışımı şeklinde piyasada satılmaktadır. Uzun etki süreleri S-enantiomerin tek başına farmakokinetiğine bağlıdır. Ayrıca ilacın dozu, plazma yarılanma ömrü, proteine bağlanma oranı ve ilacın atılım yolu da ilacın etkisini değiştirebilir (3,46,51).
Antipiretik ilaçların etkinliğinin karşılaştırıldığı bir çalışmada erişkinlerde oral ibuprofenin oral parasetamole etki süresinin benzer, fakat biraz daha güçlü antipiretik etkili olduğu gösterilmiştir. İkisinin de maksimum etkinliği oral verildikten 3-4 saat sonra oluşur. Çocuklarda yapılan bir çalışmada oral (5 mg/kg/gün) ve rektal (100-400 mg/gün) nimesulid ile oral plasebo ve rektal parasetamol (200-800 mg/gün) karşılaştırılmıştır. Bu çalışmada nimesulidin her iki formunun birbiriyle eşit etkili olduğu ve 100 mg rektal nimesulidin en az 200 mg rektal parasetamol kadar etkili olduğu gösterilmiştir. Erişkinlerde yapılan çalışmalarda da ibuprofenin (800 mg/gün) parasetamolden antipiretik olarak üstün olduğu, ketorolağın (intramusküler) parasetamol kadar etkili olduğu, oral nimesulid (200 mg) ve dipironun (500 mg) asetilsalisilik asitten (500 mg) daha etkili olduğu gösterilmiştir (3).
NSAİİ'lerin Sınıflandırılması
NSAİİ'ler kimyasal yapılarına, COX inhibisyonuna ve yarılanma sürelerine göre sınıflandırılabilir.
A. Kimyasal yapılarına göre NSAİİ'ler (51,52)
1. Karboksilik asit türevleri:
• Asetilize karboksilik asit türevleri: asetilsalisilik asit,
• Asetilize olmayan karboksilik asit türevleri: diflunisal.
2. Fenil asetik asit türevleri: diklofenak sodyum, etodolak, indometazin, sulindak, tolmetin.
3. Fenil propionik asit türevleri (profenler): fenbufen, fenoprofen, flurbiprofen, ibuprofen, ketoprofen, pirprofen.
4. Fenamik asit türevleri: flufenamik asit, meklofenamik asit, mefenamik asit.
5. Enolik asit türevleri:
• Pirazolon türevleri: fenilbutazon, oksifenil butazon, metamizol sodyum, aminopirin, propifenazon.
• Oksikam türevleri: isoksikam, piroksikam, tenoksikam, meloksikam.
6. Paraaminofenol türevleri: parasetamol, fenasetin.
7. Asidik olmayan ajanlar: nabumeton.
Paraaminofenol grubu dışında tümü analjezik, antipiretik ve antiinflamatuvar etkilidir. Paraaminofenol grubu ise antiinflamatuvar etki göstermez. Analjezik ve antipiretik etkilidir.
B. Siklooksijenaz enzim inhibisyonuna göre NSAİİ'ler: NSAİİ'lerin siklooksijenaz enzimleri üzerine etkinliği in vivo ve eks vivo yöntemlerle ölçülerek %50 inhibitör konsantrasyonları (IC50) saptanabilir. COX-1 etkinliği düşük olan ilaçların antiinflamatuvar etkinliği fazla iken, gastrik ve renal yan etkileri daha azdır. NSAİİ'lerin siklooksijenaz enzimlerine farklı seçiciliğinin saptanması sebebiyle 1999 yılında selektif siklooksijenaz inhibitörleri geliştirilmiştir (41). Siklooksijenaz enzim seçiciliğine göre de NSAİİ'ler sınıflandırılabilir (41,44). Buna göre;
1. Selektif COX-1 inhibitörleri: Düşük doz asetilsalisilik asit,
2. Selektif olmayan siklooksijenaz inhibitörleri: Yüksek doz asetilsalisilik asit, indometazin. Bu grup ilaçların COX-1/COX-2:IC50 oranı = 0.5-3'tür.
3. Rölatif selektif COX-2 inhibitörleri: Meloksikam, nimesulid, diklofenak. Bu grup ilaçların COX-1/COX-2:IC50 oranı = 10-30'dur,
4. Yüksek düzeyde selektif COX-2 inhibitörleri: Selekoksib, rofekoksib. Bu grup ilaçların COX-1/COX-2:IC50 oranı = 140-250'dir.
C. Plazma yarılanma sürelerine göre NSAİİ'ler (51):
1. Yarılanma süresi kısa (altı saatten az) olan ilaçlar: asetilsalisilik asit, diklofenak, etodolak, fenoprofen, flufenamik asit, ibuprofen, indometazin, ketoprofen, ketorolak, pirprofen, tiaprofenik asit, tolmetin.
2. Yarılanma süresi uzun olan (10 saatten fazla) ilaçlar: diflunisal, fenbufen, nabumeton, naproksen, fenilbutazon, piroksikam, salisilat, sulindak, tenoksikam.
SIK KULLANILAN ANTİPİRETİKLER
Salisilatlar
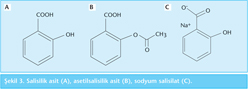
Aspirin olarak bilinen asetilsalisilik asit en çok kullanılanıdır (Şekil 3). Analjezik, antipiretik, antiinflamatuvar ve antitrombotik özelliği vardır. Asetilsalisilik asit ve benzeri antipiretiklerin esas etki mekanizması siklooksijenaz inhibisyonu yaparak PGE2 azaltmaktır. Antitrombotik etkisi de trombositler üzerindeki siklooksijenaz enzim inhibisyonuyla oluşur.
Artrit, kardit, akut romatizmal ateş gibi çeşitli inflamatuvar hastalıkların tedavisinde, ayrıca akut koroner kalp hastalığı ve kronik serebral sinovenöz tromboz tedavisinde kullanılır. Mide mukozasında erozyon, ülser ve kanamaya yol açar. Kanama nedeni karaciğerde koagülasyon faktörlerinin sentezini azaltması ve trombosit agregasyonunu inhibe etmesi sebebiyledir. Bronkospazm, vazomotor rinit, anjiyoödem gibi allerjik reaksiyonlara da yol açabilir. Nefrotoksik ve hepatotoksik etkisi de vardır (46).
Asetilsalisilik asit mideden absorbe olabilir, karaciğerde hidrolize edilir. İlaç alındıktan 1-2 saat sonra kanda hidrolize edilmeden ancak %25 oranında bulunur. Asetilsalisilik asit oral kullanılır. Analjezik etki için 4-6 saatte bir 500-750 mg tekrarlanmalı ve maksimum dozu 4 g'ı geçmemelidir (52).
Sodyum salisilat asetilsalisilik asit majör metabolitidir; analjezik, antipiretik ve antiinflamatuvar etkisi asetilsalisilik aside göre daha zayıftır (Şekil 3). Antiagregan etkisi yoktur (46). Bağırsak kaplamalı tabletler şeklinde kullanıldığı için gastrointestinal sistem mukoza hasarı yapma riski düşüktür. Plazma proteinlerine bağlanma oranı asetilsalisilik aside göre daha yüksektir (52).
Diflunisal
Salisilik asidin diflorofenil derivesidir. Analjezik, antiinflamatuvar ve antipiretik etkili olup, COX-1 ve COX-2 inhibisyonu zayıftır. Asıl iskelet-kas sistemiyle ilgili hastalıklarda analjezik etki için kullanılır. Yan etkileri diğer salisilatlara benzer (46).
Parasetamol
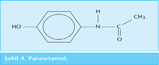
En çok kullanılan analjezik ve antipiretik ilaçlardan biridir (Şekil 4). İlk olarak 1878 yılında Morse tarafından sentezlenmiş, 1887 yılında von Mering tarafından kullanılmış, fakat o dönemde fenasetinin çok yaygın kullanılması sebebiyle fazla kullanıma girememiştir. Fenasetinin toksisitesi nedeniyle kullanımdan çekilmesiyle 1950'li yıllarda Brodie ve Axelrod tarafından yeniden keşfedilmiş ve ABD'de 1955 yılında kullanıma girmiştir (53). Parasetamol de diğer NSAİİ'lerde olduğu gibi siklooksijenaz enzimi aracılığıyla prostaglandin sentezini inhibe eder. Parasetamolün analjezik ve antipiretik etkisi asetilsalisilik aside benzer, fakat antiinflamatuvar, antiromatizmal ve antiagregan etkisi yoktur. Düz kas spazmına bağlı ağrılarda etkinliği düşüktür. Kardiyovasküler sistem ve böbrekler üzerinde toksik etkisi, solunum depresan etkisi yoktur. Parasetamol hipotalamus ve omurilik arka boynuzda prostaglandin sentezi ve salınımını inhibe ederek santral siklooksijenaz inhibisyonu yapar. Bu görüş deneysel olarak da gösterilmiştir. Köpek serebral korteksinde COX-3 veya PGHS-1b identifiye edilmiştir (54). Yapılan çalışmalarda insan ve maymunlarda COX-3'ün aminoasit diziliminin COX-1 ve COX-2'den farklı olduğu gösterilmiştir. Ateşle beraber COX-2 indüksiyonu ve PGE2 yapımı hipotalamusta artar. COX-1 veya varyant COX-1'in (COX-3) rolü buradadır (9,55). Beyin omurilik sıvısı (BOS)'nda parasetamol konsantrasyonu plazma düzeyinden daha fazla olup, ağrı ve ateş yanıtını yansıtır. Parasetamolün etki mekanizmasıyla ilgili olarak alternatif mekanizmalar da ileri sürülmüştür. Bunlar L-arjinin nitrik oksit yolu (NO), substant P veya N-metil-D aspartat (NDMA) yolu, omurilik üzerindeki inen serotonerjik ağrı yolu ve aktif parasetamol metabolitlerinin kannabinoid reseptör aktivitesi göstermesi olarak ileri sürülmüştür (54).
Parasetamolün periferik siklooksijenaz inhibisyonu etkisi zayıf olup gastrointestinal ve böbrek toksisitesi de minimaldir (3). Parasetamol asetilsalisilik aside yaklaşık eşit düzeyde analjezik ve antiinflamatuvar etkilidir. Analjezik etki için gerekli plazma düzeyi antipiretik etki için gerekli olandan daha fazladır. Erişkin dozu her dört saatte bir 650-1000 mg olacak şekilde önerilir. Maksimum günlük doz 4 g'dır. Çocuklara her 4-6 saatte bir 10-15 mg/kg önerilir ve maksimum beş doz verilmelidir. Orta düzey böbrek yetmezliğinde doz aralığı altı saate, ciddi böbrek yetmezliğinde ise sekiz saate çıkarılmalıdır. Oral alındıktan sonra 30 dakika-1 saat içinde maksimum plazma düzeyine ulaşır. Bir doz alındıktan sonra analjezik etkisi yaklaşık dört saat devam eder. Besinlerle alımı absorpsiyonunu azaltır. Oral biyoyararlanımı %60-89'dur. Parasetamol tüm vücut sıvılarına iyi dağılır, plasenta ve BOS'a geçebilir. Karaciğerde metabolize edilir. %40-67 oranında glukuronid, %20-40 sülfat ve sisteinle konjuge olur (53). Gastrointestinal sistem, kardiyovasküler sistem ve dolaşım sistemi üzerinde belirgin bir yan etkisi yoktur. Kanama zamanını uzatmaz. En önemli yan etkisi hepatotoksisitedir. Yüksek doz alındığında akut karaciğer yetmezliğinin en önemli sebebidir. Parasetamol glukuronidasyon ve sülfatyon yoluyla metabolize olarak N-asetil-p-benzokinonimin oluşmakta, aşırı olduğunda hücre proteinlerine ve DNA'ya kovalen bağlanarak akut hepatotoksisiteye yol açmaktadır (3,52). Hepatotoksik etkisi dışında ikinci önemli yan etkisi böbrekler üzerinedir ve analjezik nefropatisi yapabilir (52,53).
Fenilpropionik Asit Türevleri
Asetilsalisilik asit ve parasetamol dışında en fazla kullanılan NSAİİ'ler arasında bu grup ilaçlar yer alır. Analjezik, antipiretik ve antiinflamatuvar özellikleri vardır. Moleküler yapılarında bir kiral merkez bulunur ve S- ve R-enantiomerleri içerir. S-enantiomerin siklooksijenaz enzim inhibisyonu R-enantiomere göre daha fazladır. Her iki siklooksijenaz izoenzimini bloke eder. Gastrointestinal sistemden absorbe olur ve karaciğerde metabolize edilir. Bu grupta ibuprofen, naproksen, ketoprofen, fenbufen, tiaprofenik asit ve fenprofen bulunur (46,52).
İbuprofen: Fenilpropionik asit türevi olarak ilk bulunanıdır. Analjezik, antipiretik ve antiinflamatuvar etkinliği diğerlerine göre daha zayıftır. Romatoid artrit, osteoartrit, gut artriti tedavisinde analjezik olarak ve antipiretik olarak kullanılır. Gastrointestinal sistemde, böbreklerde toksisite ve kemik iliği depresyonu yapabilir (46).
Naproksen: Bu grup içerisinde uzun etkili analjezik, antiinflamatuvar ve antipiretik özelliği olan bir ilaçtır. İnflamasyon bölgesindeki lökosit aktivasyonunu ve migrasyonunu inhibe edici etkisi de vardır. Ayrıca, trombosit agregasyonunu inhibe ederek kanama zamanını uzatabilir. Gastrointestinal sistem irritasyonu, baş ağrısı, vertigo ve depresyon gibi yan etkileri olabilir (52).
Ketoprofen: Naproksene benzer, hem periferik hem de santral COX enzimi inhibisyonu yapar.
Fenprofen ve tiaprofen: Analjezik, antiinflamatuvar ve antipiretik etkili benzer ilaçlardır. Fenprofenin gastrointestinal yan etkileri daha azdır (46).
Selektif COX-2 İnhibitörleri
Selektif COX-2 inhibitörlerinin terapötik etkileri diğer NSAİİ'lere göre daha güçlü iken, yan etkileri daha azdır.
Meloksikam: Rölatif COX-2 inhibitörü olup, COX-2 etkisi COX-1'den daha fazladır. Fakat COX-2'ye selektivitesi yüksek dozlarda azalırken, COX-1 inhibisyonu artar. Etkisi diğer NSAİİ'lere benzer. Uzun etki sürelidir (5,46).
Nimesulid: Rölatif COX-2 inhibitörü olup, COX-2'ye etkisi COX-1'den beş kat fazladır. Yüksek dozlarda ise COX-2 selektivitesi azalır ve COX-1 etkisi artar. Antipiretik etkisi prostaglandin sentez inhibisyonuyla olur. Sindirim sistemi yan etkileri daha azdır ve antioksidan özelliği vardır (56).
Selekoksib ve rofekoksib: COX-2'ye seçiciliği fazla olan siklooksijenaz inhibitörleridir. Antiinflamatuvar etkileri güçlü, gastrointestinal sistem etkileri daha az olan ilaçlardır. Son zamanlarda kardiyovasküler problemlere yol açtıkları bildirilmektedir ve kardiyovasküler yan etkileri daha az olan yeni COX-2 inhibitörleri geliştirilmektedir. Selektif COX-2 inhibitörlerin analjezik, antipiretik, antiinflamatuvar etkileri diğer NSAİİ'ler gibidir. Fakat tromboksan A2 enzimi üzerinde inhibitör etkileri olmadığı için antitrombotik etkileri yoktur. Bu sebeple trombotik kardiyovasküler hastalıklara yol açabilir. Ayrıca, hipertansiyonu olan hastalarda kan basıncı değişikliklerine yol açabilir. Bu etki rofekoksibte selekoksibe göre daha fazladır (8,57).
Sonuç olarak; infeksiyon hastalıkları uygulamalarında antipiretik kullanımı daha çok hekim kanaatine bağlı olarak olgunlaşması gereken bir endikasyondur. Hasta bireysel olarak değerlendirilmeli ve buna bağlı olarak ateşin düşürülme ya da düşürülmeme kararı verilmelidir.
KAYNAKLAR
- Mackowiak PA. Editorial response: assaulting a physiological response. Clin Infect Dis 1997; 24: 1214-6.
- Neymann C, Osborne, SL. Artificial fever. Am J Syphilis Neurol 1934: 18-34.
- Plaisance KI, Mackowiak PA. Antipyretic therapy: physiologic rationale, diagnostic implications, and clinical consequences. Arch Intern Med 2000; 160: 449-56.
- Mackowiak PA. Brief history of antipyretic therapy. Clin Infect Dis 2000; 31(Suppl 5): S154-6.
- Botting R. Antipyretic therapy. Front Biosci 2004; 9: 956-66.
- Jack DB. One hundred years of aspirin. Lancet 1997; 350: 437-9.
- Jones R. Non-Steroidal anti-inflammatory drug prescribing: past, present, and future. Am J Med 2001; 110(1A): 4S-7S.
- Simmons DL, Wagner D, Westover K. Non-steroidal anti-inflammatory drugs, acetaminophen, cyclooxygenase 2, and fever. Clin Infect Dis 2000; 31(Suppl 5): S211-8.
- Rainsford KD. Anti-inflammatory drugs in the 21st century. Subcell Biochem 2007; 42: 3-27.
- Lessell S, Torres JM, Kurland LT. Seizure disorders in a Guamanian village. Arch Neurol 1962; 7: 37-44.
- Aicardi J. Febrile convulsions. In: Aicardi JE (ed). Epilepsy in Children. 2nd ed. New York: Raven Press, 1994: 253-75.
- Lennox-Buchthal MA. Febrile Convulsions. A Reappraisal. Amsterdam: Elsevier, 1973.
- Rosman NP. Febrile convulsions. In: Mackowiak PA (ed). Fever: Basic Mechanisms and Management. 2nd ed. Philadelphia: Lippincott-Raven, 1997: 267-77.
- Camfield PR, Camfield CS, Shapiro SH, Cummings C. The first febrile seizure-antipyretic instruction plus either phenobarbital or placebo to prevent recurrence. J Paediatr 1980; 97: 16-21.
- Uhari M, Rantala H, Vainionpaa L, Kurttila R. Effect of acetaminophen and of low intermittent doses of diazepam on prevention of recurrences of febrile seizures. J Pediatr 1995; 126: 991-5.
- Schnaiderman D, Lahat E, Sheefer T, Aladjem M. Antipyretic effectiveness of acetaminophen in febrile seizures: ongoing prophylaxis versus sporadic usage. Eur J Pediatr 1993; 152: 747-9.
- Styrt B, Sugarman B. Antipyresis and fever. Arch Intern Med 1990; 150: 1589-97.
- Greisman SE. Cardiovascular alterations during fever In: Mackowiak PA (ed). Fever: Basic Mechanisms and Management. New York: Raven Press, 1991: 143-65.
- Mackowiak PA. Temperature regulation and the pathogenesis of fever. In: Mandell GL, Bennett JE, Dolin R (eds). Mandell, Douglass, and Bennett's Principles and Practice of Infectious Diseases. 7th ed. Philadelphia: Churchill Livingstone, 2010: 765-78.
- Dorn TF, De Angelis C, Baumgardner RA, et al. Acetaminophen: more harm than good for chicken pox? J Pediatr 1989; 114: 1045-8.
- Stanley ED, Jackson GG, Panusarn C, Rubenis M, Dirda V. Increased virus shedding with aspirin treatment of rhinovirus infection. JAMA 1975; 231: 1248-51.
- Graham MH, Burrell CJ, Douglas RM. Adverse effects of aspirin, acetaminophen, and ibuprofen on immune function, viral shedding, and clinical status in rhinovirus-infected volunteers. J Infect Dis 1990; 162: 1277-82.
- Plaisance KI, Kudaravalli S, Wasserman SS, Levine MM, Mackowiak PA. Effect of antipyretic therapy on the duration of illness in experimental influenza A, Shigella sonnei, and Rickettsia rickettsii infections. Pharmacotherapy 2000; 20: 1417-22.
- Friedman PL, Brown EJ Jr, Gunther S, et al. Coronary vasoconstrictor effect of indomethacin in patients with coronary-artery disease. N Engl J Med 1981; 305: 1171-5.
- Mukherjee D, Nissen SE, Topol EJ. Risk of cardiovascular events associated with selective COX-2 inhibitors. JAMA 2001; 286: 954-9.
- Bernard GR, Wheeler AP, Russell JA, et al. The effects of ibuprofen on the physiology and survival of patients with sepsis. The Ibuprofen in Sepsis Study Group. N Engl J Med 1997; 336: 912-8.
- Eichacker PQ, Parent C, Kalil A, et al. Risk and the efficacy of antiinflammatory agents: retrospective and confirmatory studies of sepsis. Am J Respir Crit Care Med 2002; 166: 1197-205.
- Manthous CA, Hall JB, Olson D, et al. Effect of cooling on oxygen consumption in febrile critically ill patients. Am J Respir Crit Care Med 1995; 151: 10-4.
- Raizner AE, Chahine RA, Ishimori T, et al. Provocation of coronary artery spasm by the cold pressor test. Hemodynamic, arteriographic and quantitative angiographic observations. Circulation 1980; 62: 925-32.
- Nabel EG, Ganz P, Gordon JB, et al. Dilation of normal and construction of atherosclerotic coronary arteries caused by the cold pressor test. Circulation 1987; 77: 43-52.
- Lenhardt R, Kurz A, Sessler DI. Thermoregulation and hyperthermia. Acta Anaesthesiol Scand 1996; 109(Suppl): 34-8.
- Kluger MJ, Kozak W, Conn CA, et al. The adaptive value of fever. In: Mackowiak PA (ed). Fever: Basic Mechanisms and Management. 2nd ed. Philadelphia: Lippincott-Raven, 1997: 255-66.
- Mackowiak PA, Plaisance KI. Benefits and risks of antipyretic therapy. Ann N Y Acad Sci 1998; 856: 214-23.
- Sullivan JE, Farrar HC. Fever and antipyretic use in children. Pediatrics 2011; 127: 580-7.
- Kayman H. Management of fever: making evidence-based decisions. Clin Pediatr (Phila) 2003; 42: 383-92.
- Prymula R, Siegrist CA, Chlibek R, et al. Effect of prophylactic paracetamol administration at time of vaccination on febrile reactions and antibody responses in children: two open-label, randomised controlled trials. Lancet 2009; 374: 1339-50.
- Kett DH, Breitmeyer JB, Ang R, Royal MA. A randomized study of the efficacy and safety of intravenous acetaminophen vs. intravenous placebo for the treatment of fever. Clin Pharmacol Ther 2011; 90: 32-9.
- Sarrell EM, Wielunsky E, Cohen HA. Antipyretic treatment in young children with fever: acetaminophen, ibuprofen, or both alternating in a randomized, double-blind study. Arch Pediatr Adolesc Med 2006; 160: 197-202.
- Dinarello CA. Cytokines as endogenous pyrogens. In: Mackowiak PA (ed). Fever: Basic Mechanisms and Management. 2nd ed. Philadelphia: Lippincott-Raven, 1997: 87-116.
- Vane JR, Botting RM. New insights into the mode of action of anti-inflammatory drugs. Inflamm Res 1995; 44: 1-10.
- Botting RM. Inhibitors of cyclooxygenases: mechanisms, selectivity and uses. J Physiol Pharmacol 2006; 57 (Suppl 5): S113-24.
- Botting RM. Vane's discovery of the mechanism of action of aspirin changed our understanding of its clinical pharmacology. Pharmacol Rep 2010; 62: 518-25.
- Dannhardt G, Kiefer W. Cyclooxygenase inhibitors-current status and future prospects. Eur J Med Chem 2001; 36: 109-26.
- Cronstein BN. Cyclooxygenase-2-selective inhibitors: translating pharmacology into clinical utility. Cleve Clin J Med 2002; 69(Suppl 1): S13-9.
- Rao P, Knaus EE. Evolution of non-steroidal anti-inflammatory drugs (NSAIDs): cyclooxygenase (COX) inhibition and beyond. J Pharm Pharm Sci 2008; 11: 81-110.
- Suleyman H, Demircan B, Karagoz Y. Anti-inflammatory and side effects of cyclooxygenase inhibitors. Pharmacol Rep 2007; 59: 247-58.
- Smith WL, Langenbach R. Why there are two cyclooxygenase isozymes. J Clin Invest 2001; 107: 1491-5.
- Vonkeman HE, van de Laar MA. Non-steroidal anti-inflammatory drugs: adverse effects and their prevention. Semin Arthritis Rheum 2010; 39: 294-312.
- Botting R, Ayoub SS. COX-3 and the mechanism of action of paracetamol/acetaminophen. Prostaglandins Leukot Essent Fatty Acids 2005; 72: 85-7.
- Aronoff DM, Neilson EG. Antipyretics: mechanisms of action and clinical use in fever suppression. Am J Med 2001; 111: 304-15.
- Brooks P. Use and benefits of non-steroidal anti-inflammatory drugs. Am J Med 1998; 104: 9-13.
- Kayaalp O MM. Nonsteroidal antiinflamatuar ilaçlar. Kayaalp O (editör). Rasyonel Tedavi Yönünden Tıbbi Farmakoloji. 9. Baskı. Ankara: Hacettepe Taş Yayınları, 2000: 1026-62.
- Bertolini A, Ferrari A, Ottani A, Guerzoni S, Tacchi R, Leone S. Paracetamol: new vistas of an old drug. CNS Drug Rev 2006; 12: 250-75.
- Anderson BJ. Paracetamol (acetaminophen): mechanisms of action. Paediatr Anaesth 2008; 18: 915-21.
- Botting RM. Mechanism of action of acetaminophen: is there a cyclooxygenase 3? Clin Infect Dis 2000; 31(Suppl 5): S202-10.
- Chandra J, Bhatnagar SK. Antipyretics in children. Indian J Pediatr 2002; 69: 69-74.
- Risser A, Donovan D, Heintzman J, Page T. NSAID prescribing precautions. Am Fam Physician 2009; 80: 1371-8.
Yazışma Adresi:
Doç. Dr. Serap GENÇER
Dr. Lütfi Kırdar Kartal Eğitim ve
Araştırma Hastanesi,
İnfeksiyon Hastalıkları ve
Klinik Mikrobiyoloji Kliniği,
İSTANBUL
E-posta: gencerse@gmail.com